Что такое периодическая система. Периодическая система менделеева.
Периодическая система химических элементов (табли́ца Менделе́ева) - классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра. Система является графическим выражением периодического закона, установленного русским химиком Д. И. Менделеевым в 1869 году. Её первоначальный вариант был разработан Д. И. Менделеевым в 1869-1871 годах и устанавливал зависимость свойств элементов от их атомного веса (по-современному, от атомной массы). В современном варианте системы предполагается сведение элементов в двумерную таблицу, в которой каждый столбец (группа) определяет основные физико-химические свойства, а строки представляют собой периоды, в определённой мере подобные друг другу.
Классический вид таблицы Менделеева
История открытия Периодического закона.
К середине XIX века были открыты 63 химических элемента, и попытки найти закономерности в этом наборе предпринимались неоднократно.
В 1829 году Дёберейнер опубликовал найденный им «закон триад»: атомный вес многих элементов близок к среднему арифметическому двух других элементов, близких к исходному по химическим свойствам (стронций, кальций и барий; хлор, бром и йод и др.). Первую попытку расположить элементы в порядке возрастания атомных весов предпринял Александр Эмиль Шанкуртуа (1862), который разместил элементы вдоль винтовой линии и отметил частое циклическое повторение химических свойств по вертикали. Обе указанные модели не привлекли внимания научной общественности.
В 1866 году свой вариант периодической системы предложил химик и музыкант Джон Александр Ньюлендс, модель которого («закон октав») внешне немного напоминала менделеевскую, но была скомпрометирована настойчивыми попытками автора найти в таблице мистическую музыкальную гармонию. В этом же десятилетии появились ещё несколько попыток систематизации химических элементов; ближе всего к окончательному варианту подошёл Юлиус Лотар Мейер (1864). Д. И. Менделеев опубликовал свою первую схему периодической таблицы в 1869 году в статье «Соотношение свойств с атомным весом элементов» (в журнале Русского химического общества); ещё ранее (февраль 1869 г.) научное извещение об открытии было им разослано ведущим химикам мира.
По легенде, мысль о системе химических элементов пришла к Менделееву во сне, однако известно, что однажды на вопрос, как он открыл периодическую систему, учёный ответил: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово».
Написав на карточках основные свойства каждого элемента (их в то время было известно 63, из которых один - дидим Di - оказался в дальнейшем смесью двух вновь открытых элементов празеодима и неодима), Менделеев начинает многократно переставлять эти карточки, составлять из них ряды сходных по свойствам элементов, сопоставлять ряды один с другим. Итогом работы стал отправленный в 1869 году в научные учреждения России и других стран первый вариант системы («Опыт системы элементов, основанной на их атомном весе и химическом сходстве»), в котором элементы были расставлены по девятнадцати горизонтальным рядам (рядам сходных элементов, ставших прообразами групп современной системы) и по шести вертикальным столбцам (прообразам будущих периодов). В 1870 году Менделеев в «Основах химии» публикует второй вариант системы («Естественную систему элементов»), имеющий более привычный нам вид: горизонтальные столбцы элементов-аналогов превратились в восемь вертикально расположенных групп; шесть вертикальных столбцов первого варианта превратились в периоды, начинавшиеся щелочным металлом и заканчивающиеся галогеном. Каждый период был разбит на два ряда; элементы разных вошедших в группу рядов образовали подгруппы.
Сущность открытия Менделеева заключалась в том, что с ростом атомной массы химических элементов их свойства меняются не монотонно, а периодически. После определённого количества разных по свойствам элементов, расположенных по возрастанию атомного веса, свойства начинают повторяться. Например, натрий похож на калий, фтор похож на хлор, а золото похоже на серебро и медь. Разумеется, свойства не повторяются в точности, к ним добавляются и изменения. Отличием работы Менделеева от работ его предшественников было то, что основ для классификации элементов у Менделеева была не одна, а две - атомная масса и химическое сходство. Для того, чтобы периодичность полностью соблюдалась, Менделеевым были предприняты очень смелые шаги: он исправил атомные массы некоторых элементов (например, бериллия, индия, урана, тория, церия, титана, иттрия), несколько элементов разместил в своей системе вопреки принятым в то время представлениям об их сходстве с другими (например, таллий, считавшийся щелочным металлом, он поместил в третью группу согласно его фактической максимальной валентности), оставил в таблице пустые клетки, где должны были разместиться пока не открытые элементы. В 1871 году на основе этих работ Менделеев сформулировал Периодический закон, форма которого со временем была несколько усовершенствована.
Научная достоверность Периодического закона получила подтверждение очень скоро: в 1875-1886 годах были открыты галлий (экаалюминий), скандий (экабор) и германий (экасилиций), для которых Менделеев, пользуясь периодической системой, предсказал не только возможность их существования, но и, с поразительной точностью, целый ряд физических и химических свойств.
Список химических элементов таблицы Менделеева
- 1 H Водород (а.м. 1,00794)
- 2 He Гелий (а.м. 4,002602)
- 3 Li Литий (а.м. 6,9412)
- 4 Be Бериллий (а.м. 9,0122)
- 5 B Бор (а.м. 10,812)
- 6 С Углерод (а.м. 12,011)
- 7 N Азот (а.м. 14,0067)
- 8 О Кислород (а.м. 15,9994)
- 9 F Фтор (а.м. 18,9984)
- 10 Ne Неон (а.м. 20,179)
- 11 Na Натрий (а.м. 22,98977)
- 12 Mg Магний (а.м. 24,305)
- 13 Al Алюминий (а.м. 26,98154)
- 14 Si Кремний (а.м. 28,086)
- 15 P Фосфор (а.м. 30,97376)
- 16 S
Он опирался на труды Роберта Бойле и Антуана Лавузье. Первый ученый ратовал за поиск неразложимых химических элементов. 15 из таковых Бойле перечислил еще в 1668-ом году.
Лавузье прибавил к ним еще 13, но спустя век. Поиски растянулись, поскольку не было стройной теории связи между элементами. Наконец, в «игру» вступил Дмитрий Менделеев. Он решил, что есть связь между атомной массой веществ и их местом в системе.
Эта теория позволила ученому открыть десятки элементов, не обнаруживая их на практике, а природе. Это было возложено на плечи потомков. Но, сейчас не о них. Посвятим статью великому русскому ученому и его таблице.
История создания таблицы Менделеева
Таблица Менделеева началась с книги «Соотношение свойств с атомным весом элементов». Труд выпущен в 1870-ых. Тогда же русский ученый выступил перед химическим обществом страны и разослал первый вариант таблицы коллегам из-за рубежа.
До Менделеева разными учеными были открыты 63 элемента. Наш соотечественник начал со сравнения их свойств. В первую очередь, работал с калием и хлором. Потом, взялся за группу металлов щелочной группы.
Химик обзавелся специальным столом и карточками элементов, чтобы раскладывать их, как пасьянс, ища нужные совпадения и комбинации. В итоге, пришло прозрение: — свойства компонентов зависят от массы их атомов. Так, элементы таблицы Менделеева выстроились в ряды.
Находкой маэстро химии стало решение оставить в этих рядах пустоты. Периодичность перепада между атомными массами заставила ученого предположить, что человечеству известны еще не все элементы. Промежутки в весе между некоторыми «соседями» были слишком велики.

Поэтому, периодическая таблица Менделеева стала похожа на шахматное поле, с обилием «белых» клеток. Время показало, что они, действительно, ждали своих «постояльцев». Ими, к примеру, стали инертные газы. Гелий, неон, аргон, криптон, радиоакт и ксенон открыты лишь в 30-ых годах 20-го века.
Теперь о мифах. Распространено мнение, что химическая таблица Менделеева явилась ему во сне. Это происки университетских педагогов, точнее, одного из них – Александра Иностранцева. Это русский геолог, читавший лекции в Петербургском университете горного дела.
Иностранцев был знаком с Менделеевым, бывал у него в гостях. Однажды, изможденный поисками Дмитрий заснул прямо при Александе. Тот дождался, пока химик проснется и увидел, как Менделеев хватается за листок и записывает окончательный вариант таблицы.
По сути, ученый просто не успел сделать это до того, как его захватил Морфей. Однако, Иностранцеву хотелось позабавить своих студентов. На основе виденного геолог придумал байку, которую благодарные слушатели быстро распространили в массы.
Особенности таблицы Менделеева
С момента первой версии 1969-го года порядковая таблица Менделеева не раз дорабатывалась. Так, с открытием в 1930-ых благородных газов удалось вывести новую зависимость элементов, — от их порядковых номеров, а не массы, как заявлял автор системы.
Понятие «атомный вес» заменили на «атомный номер». Удалось изучить число протонов в ядрах атомов. Эта цифра и есть порядковый номер элемента.
Ученые 20-го века изучили и электронное строение атомов. Оно тоже влияет на периодичность элементов и отражено в поздних редакциях таблицы Менделеева. Фото списка демонстрирует, что вещества в нем расставлены по мере роста атомного веса.
Первооснову менять не стали. Масса увеличивается слева направо. При этом, таблица не едина, а поделена на 7 периоды. Отсюда и название списка. Период – горизонтальный ряд. Его начало – типичные металлы, конец – элементы с неметаллическими свойствами. Убывание постепенное.
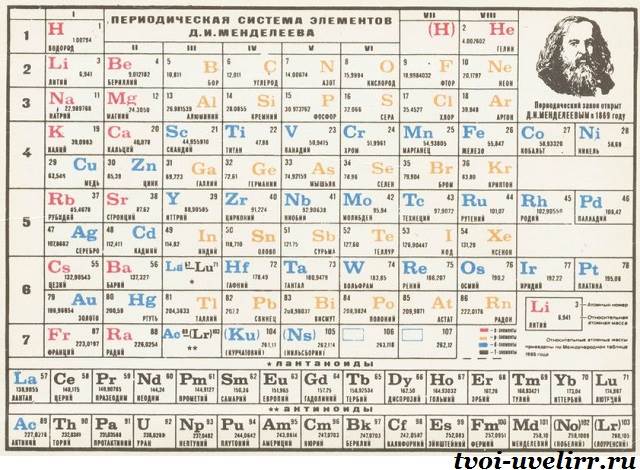
Есть большие и малые периоды. Первые находятся в начале таблицы, их 3. Открывает список период из 2-х элементов. Следом идут две колонки, в которых по 8 наименований. Оставшиеся 4 периода большие. Наиболее протяжен 6-ой, в нем 32 элемента. В 4-ом и 5-ом их по 18, а в 7-ом – 24.
Можно сосчитать, сколько элементов в таблице Менделеева. Всего 112 наименований. Именно наименований. Клеток же 118, а есть вариации списка и со 126-ю полями. Все еще остаются пустые клетки для неоткрытых элементов, не имеющих имен.
Не все периоды умещаются в одну строку. Большие периоды состоят из 2-х рядов. Количество металлов в них перевешивает. Поэтому, им полностью посвящены нижние строки. Постепенное убывание от металлов к инертным веществам соблюдается в верхних рядах.
Картинки таблицы Менделеева поделены и вертикально. Это группы в таблице Менделеева , их 8. Вертикально скомпонованы элементы, схожие по химическим свойствам. Они поделены на главную и побочную подгруппы. Последние начинаются только с 4-го периода. В главные подгруппы входят и элементы малых периодов.
Суть таблицы Менделеева
Названия элементов в таблице Менделеева – это 112 позиций. Суть их компоновки в единый список – систематизация первоэлементов. Над этим начали биться еще в античные времена.
Одним из первых понять, из чего составлено все сущее попытался Аристотель. Он взял за основу свойства веществ – холод и тепло. Эмпидокл выделил 4-ре первоосновы по стихиям: воду, землю, огонь и воздух.
Металлы в таблице Менделеева , как и другие элементы, — те самые первоосновы, но с современной точки зрения. Российскому химику удалось открыть большинство составляющих нашего мира и предположить существование еще неизвестных первоэлементов.

Получается, что произношение таблицы Менделеева – озвучивание некой модели нашей реальности, раскладывание ее на составляющие. Однако, выучить их не так-то просто. Попробуем облегчить задачу, описав пару эффективных методов.
Как выучить таблицу Менделеева
Начнем с современного метода. Компьютерщиками разработан ряд флеш-игр, помогающих запомнить список Менделеева. Участникам проекта предлагают находить элементы по разным опциям, например, названию, атомной массе, буквенному обозначению.
Игрок имеет право выбрать поле деятельности – лишь часть таблицы, или ее всю. В нашей воле, так же, исключить имена элементов, другие параметры. Это усложняет поиск. Для продвинутых предусмотрен и таймер, то есть тренировка ведется на скорость.
Игровые условия делают изучение номеров элементов в таблице Менднлеева не нудным, а занятным. Просыпается азарт, и систематизировать знания в голове становится проще. Те же, кто не приемлет компьютерных флеш-проектов, предлагают более традиционный способ заучивания списка.
Его делят на 8 групп, или 18 (в соответствии с редакцией 1989-го года). Для удобства запоминания, лучше создать несколько отдельных таблиц, а не работать по цельному варианту. Помогают и зрительные образы, подобранные к каждому из элементов. Опираться следует на собственные ассоциации.
Так, железо в мозгу может соотноситься, к примеру, с гвоздем, а ртуть – с градусником. Название элемента незнакомо? Пользуемся методом наводящих ассоциаций. , например, составим из начал слов «ириска» и «динамик».
Характеристика таблицы Менделеева не учиться в один присест. Рекомендованы занятия по 10-20 минут в день. Начинать рекомендована с запоминания лишь основных характеристик: названия элемента, его обозначения, атомной массы и порядкового номера.
Школьники предпочитают вешать таблицу Менделеева над рабочим столом, или на стене, на которую часто смотрят. Метод хорош для людей с преобладанием зрительной памяти. Данные из списка невольно запоминаются даже без зубрежки.
Это учитывают и педагоги. Как правило, они не заставляют заучивать список, разрешают смотреть в него даже на контрольных. Постоянное заглядывание в таблицу равнозначно эффекту распечатки на стене, или написанию шпаргалок до экзаменов.
Приступая к изучению, вспомним, что и Менделеев не сразу запомнил свой список. Однажды, когда ученого спросили, как он открыл таблицу, последовал ответ: — «Я над ней, может, 20 лет думал, а вы считаете: сидел и, вдруг, готово». Периодическая система – кропотливый труд, который не осилить в сжатые сроки.

Наука не терпит спешки, ведь она приводит к заблуждениям и досадным ошибкам. Так, одновременно с Менделеевым таблицу составил и Лотар Мейер. Однако, немец немного недоработал список и не был убедителен при доказательстве своей точки зрения. Поэтому, общественность признала труд русского ученого, а не его коллеги-химика из Германии.
Еще в школе, сидя на уроках химии, все мы помним таблицу на стене класса или химической лаборатории. Эта таблица содержала классификацию всех известных человечеству химических элементов, тех фундаментальных компонентов, из которых состоит Земля и вся Вселенная. Тогда мы и подумать не могли, что периодическая таблица бесспорно является одним из величайших научных открытий, который является фундаментом нашего современного знания о химии.
На первый взгляд, ее идея выглядит обманчиво просто: организовать элементы в порядке возрастания веса их атомов. Причем в большинстве случаев оказывается, что химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом. Эта закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу. Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме. Разумеется, сегодня мы пользуемся понятием атомного числа (количества протонов) для того, чтобы упорядочить систему элементов. Это помогло решить так называемую техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
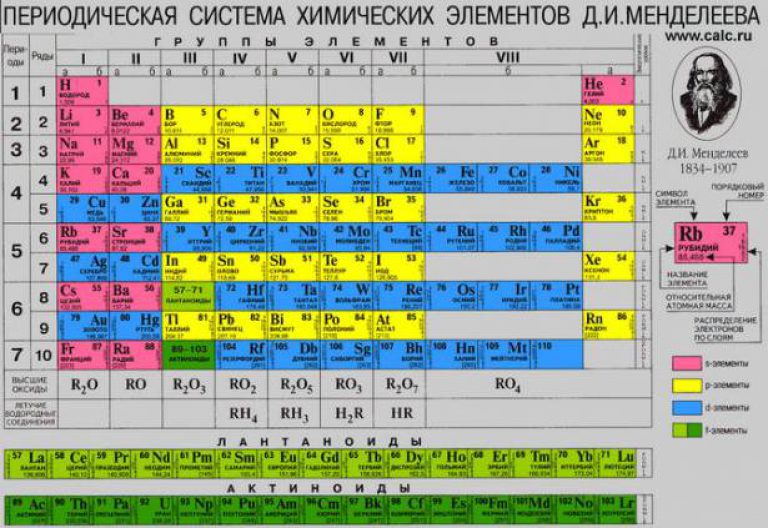
В периодической таблице все элементы упорядочены с учетом их атомного числа, электронной конфигурации и повторяющихся химических свойств. Ряды в таблице называются периодами, а столбцы группами. В первой таблице, датируемой 1869 годом, содержалось всего 60 элементов, теперь же таблицу пришлось увеличить, чтобы поместить 118 элементов, известных нам сегодня.

Свойства периодической системы Менделеева
Периодическая таблица систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).

Заглянем еще раз в Периодическую таблицу. Помимо глубокой фундаментальной связи между элементами, она отражает ряд полезных для изучения химии закономерностей.
Периоды
- горизонтальные строки химических элементов.
Группы
- вертикальные столбцы химических элементов.
Подгруппы
- А - главные (s- и р-элементы) и В - побочные (d- и f-элементы).
Номер периода
- номер внешнего энергетического уровня в электронной формуле атома элемента.
Номер группы
(для большинства элементов) - общее число валентных электронов (электронов внешнего энергетического уровня, а также предпоследнего d-подуровня, если он застроен не полностью).
Число элементов в периоде
- максимальная емкость соответствующего энергетического уровня:
1 период - 2 элемента (1s2 )
2 период - 8 элементов (2s2 2p6 )
3 период - 8 элементов (3s2 3p6 )
4 период - 18 элементов (4s2 3d10 4p6 )
5 период - 18 элементов (5s2 4d10 5p6 )
6 период - 32 элемента (6s2 4f14 5d10 6p6 )
7 период - не завершен
Построение периодов
- в начале: два s-элемента, в конце: шесть р- элементов. В четвертом и пятом периодах между ними помещается по десять d-элементов, а в шестом и седьмом к ним добавляются четырнадцать f-элементов (формы электронных орбиталей).
В периоде
- свойства химических элементов различаются между собой, так как электронные конфигурации валентных электронов их атомов различны.
В подгруппе
- свойства элементов сходны между собой, так как электронные конфигурации валентных электронов их атомов сходны. Причина периодичности свойств химических элементов заключается в периодической повторяемости сходных электронных конфигураций внешних энергетических уровней.

КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ ПО СВОЙСТВАМ
ЩЕЛОЧНЫЕ И ЩЕЛОЧНОЗЕМЕЛЬНЫЕ ЭЛЕМЕНТЫ
К ним относятся элементы из первой и второй группы периодической таблицы. Щелочные металлы из первой группы — мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним-единственным электроном на внешней оболочке и прекрасно вступают в реакцию. Щелочноземельные металлы из второй группы также имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами. По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах.
ЛАНТАНИДЫ (РЕДКОЗЕМЕЛЬНЫЕ ЭЛЕМЕНТЫ) И АКТИНИДЫ
Лантаниды — это группа элементов, изначально обнаруженных в редко встречающихся минералах; отсюда их название "редкоземельные" элементы. Впоследствии выяснилось, что данные элементы не столь редки, как думали вначале, и поэтому редкоземельным элементам было присвоено название лантаниды. Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов. Обе группы включают в себя металлы; все лантаниды (за исключением прометия) нерадиоактивны; актиниды, напротив, радиоактивны.
ГАЛОГЕНЫ И БЛАГОРОДНЫЕ ГАЗЫ
Галогены и благородные газы объединены в группы 17 и 18 периодической таблицы. Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке. В благородных газах все электроны находятся во внешней оболочке, таким образом с трудом участвуют в образовании соединений. Эти газы называют «благородными, потому что они редко вступают в реакцию с прочими элементами; т. е. ссылаются на представителей благородной касты, которые традиционно сторонились других людей в обществе.
ПЕРЕХОДНЫЕ МЕТАЛЛЫ
Переходные металлы занимают группы 3—12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны (при помощи которых они соединяются с другими элементами) находятся в нескольких электронных оболочках.
| Переходные металлы |
| Скандий Sc 21 |
| Титан Ti 22 |
| Ванадий V 23 |
| Хром Cr 24 |
| Марганец Mn 25 |
| Железо Fe 26 |
| Кобальт Co 27 |
| Никель Ni 28 |
| Медь Cu 29 |
| Цинк Zn 30 |
| Иттрий Y 39 |
| Цирконий Zr 40 |
| Ниобий Nb 41 |
| Молибден Mo 42 |
| Технеций Tc 43 |
| Рутений Ru 44 |
| Родий Rh 45 |
| Палладий Pd 46 |
| Серебро Ag 47 |
| Кадмий Cd 48 |
| Лютеций Lu 71 |
| Гафний Hf 72 |
| Тантал Ta 73 |
| Вольфрам W 74 |
| Рений Re 75 |
| Осмий Os 76 |
| Иридий Ir 77 |
| Платина Pt 78 |
| Золото Au 79 |
| Ртуть Hg 80 |
| Лоуренсий Lr 103 |
| Резерфордий Rf 104 |
| Дубний Db 105 |
| Сиборгий Sg 106 |
| Борий Bh 107 |
| Хассий Hs 108 |
| Мейтнерий Mt 109 |
| Дармштадтий Ds 110 |
| Рентгений Rg 111 |
| Коперниций Cn 112 |
МЕТАЛЛОИДЫ
Металлоиды занимают группы 13—16 периодической таблицы. Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат.
ПОСТПЕРЕХОДНЫЕ МЕТАЛЛЫ
Элементы, называемые постпереходными металлами , относятся к группам 13—15 периодической таблицы. В отличие от металлов, они не имеют блеска, а имеют матовую окраску. В сравнении с переходными металлами постпереходные металлы более мягкие, имеют более низкую температуру плавления и кипения, более высокую электроотрицательность. Их валентные электроны, с помощью которых они присоединяют другие элементы, располагаются только на внешней электронной оболочке. Элементы группы постпереходных металлов имеют гораздо более высокую температуру кипения, чем металлоиды.
НЕМЕТАЛЛЫ
Из всех элементов, классифицируемых как неметаллы , водород относится к 1-й группе периодической таблицы, а остальные — к группам 13—18. Неметаллы не являются хорошими проводниками тепла и электричества. Обычно при комнатной температуре они пребывают в газообразном (водород или кислород) или твердом состоянии (углерод).
Отлично, первый шаг на пути к знаниям сделан. Теперь вы более-менее ориентируетесь в таблице Менделеева и это вам очень даже пригодится, ведь Периодическая система Менделеева является фундаментом, на котором стоит эта удивительная наука.
Одной из самых популярных таблиц в мире является таблица Менделеева. В каждой ячейке вписаны названия химических элементов. Для ее разработки было приложено много усилий. Ведь это не просто список веществ. Они упорядочены согласно своим свойствам и особенностям. А сколько элементов в таблице Менделеева мы сейчас и узнаем.
История создания таблицы
Менделеев не был первым ученым, который решил структурировать элементы. Пытались многие. Вот только никто не мог сопоставить все в одной слаженной таблице. Датой открытия периодического закона мы можем назвать 17 февраля 1869 года. В этот день Менделеев показал свое творение – целую систему элементов, упорядоченных на основе атомного веса и химических особенностях.
Стоит отметить, что гениальная мысль не пришла ученому в один удачный вечер во время работы. Он действительно трудился около 20 лет. Снова и снова перебирал карточки с элементами, изучал их характеристики. В это же время трудились и другие ученые.
Химик Канниццаро предложил от своего имени теорию атомного веса. Он утверждал, что именно эти данные могут построить все вещества в нужном порядке. Дальше ученые Шантуркуа и Ньюлендс, работая в разных точках мира, пришли к умозаключению, что размещая элементы по атомному весу, они начинают дополнительно объединяться и по другим свойствам.
В 1869 году вместе с Менделеевым были представлены другие примеры таблиц. Но сегодня мы даже не помним имена их авторов. Почему так? Все дело в превосходстве ученого над своими конкурентами:
- Таблица имела большее количество открытых элементов, чем у других.
- Если какой-то элемент не подходил по атомному весу, ученый помещал его на основе других свойств. И это было правильным решением.
- В таблице было много пустых мест. Менделеев сделал пропуски осознано, забрав тем самым частичку славы тех, кто в будущем найдет эти элементы. Он даже дал описание некоторых еще неведомых веществ.
Самое главное достижение в том, что эта таблица неразрушима. Она создано так гениально, что любые открытия в будущем будут ее только дополнять.
Сколько элементов в таблице Менделеева
Каждый человек хотя бы раз в жизни видел эту таблицу. Но вот назвать точное количество веществ сложно. Правильных ответов может быть два: 118 и 126. Сейчас мы разберемся, почему так.
В природе люди обнаружили 94 элемента. Они ничего с ними не делали. Только изучали их свойства и особенности. Большая часть из них была в первоначальной периодической таблице.
Другие 24 элемента были созданы в лабораториях. Всего получается 118 штук. Еще 8 элементов являются лишь гипотетическими вариантами. Их пытаются изобрести или получить. Так что на сегодняшний день и вариант с 118 элементами, и с 126 элементами можно смело называть.
- Ученый был семнадцатым ребенком в семье. Восемь из них погибли еще в раннем возрасте. Отец рано ушел из жизни. Но мать продолжала бороться за будущее своих детей, так что смогла пристроить их в хорошие учебные заведения.
- Всегда отстаивал свое мнение. Был уважаемым педагогом в университетах Одессы, Симферополя и Санкт-Петербурга.
- Он никогда не изобретал водку. Алкогольный напиток был создан задолго до ученого. Но его докторская была посвящена спирту, отсюда и развилась легенда.
- Периодическая система никогда не снилась Менделееву. Она стала результатом тяжелой работы.
- Он любил делать чемоданы. И довел свое хобби до высокого уровня мастерства.
- За всю свою жизнь Менделеев 3 раза мог получить Нобелевскую премию. Но все закончилось лишь номинациями.
- Многих это удивит, то работы в области химии занимают лишь 10% всех занятий ученого. Также он изучал аэростаты и кораблестроение.

Таблица Менделеева – это удивительная система всех элементов, которые когда-либо были обнаружены людьми. Она делится на ряды и столбцы, чтобы упростить изучение всех элементов.
P.S. Статья — Сколько элементов в таблице Менделеева, опубликована в рубрике — .
Одни из самых популярных химических вопросов: "Сколько сейчас известно химических элементов?", "Сколько существует химических элементов?", "Кто их открыл?"
Эти вопросы не имеют простого и однозначного ответа.
Что значит "известно"? Встречаются в природе? На земле, в воде, в космосе? Получены и изучены их свойства? Свойства чего? Вещества в виде фаз или только на атомно-молекулярном уровне? Имеющиеся современные технологии позволяют обнаруживать и несколько атомов... Но, по отдельному атому свойства вещества не определить.
А что значит "существуют"? В практическом плане это понятно: наличествуют в природе в таком количестве и столько времени, чтобы они и их соединения могли оказывать реальное влияние на природные явления. Или хотя бы можно было изучить их свойства в лаборатории.
Таковых химических элементов в природе выявлено около 90. Почему около? Потому, что среди элементов с порядковым номером менее 92 (до урана) в природе отсутствуют технеций (43) и франций (87). Практически нет астата (85).С другой стороны, и нептуний (93) и плутоний (94) (нестабильные трансурановые элементы) обнаруживаются в природе там, где встречаются урановые руды. Все элементы следующие после плутония Pu в периодической системе Д.И.Менделеева в земной коре полностью отсутствуют, хотя некоторые из них несомненно образуются в космосе во время взрывов сверхновых звёзд. Но долго они не живут...
К настоящему времени ученые синтезировали 26 трансурановых элементов, начиная с нептуния (N=93) и заканчивая элементом с номером N=118 (номер элемента соответствует числу протонов в ядре атома и числу электронов вокруг ядра атома).
Трансурановые химические элементы от 93 до 100 получают в ядерных реакторах, а остальные - в результате ядерных реакций на ускорителях частиц. Технология получения трансурановых элементов на ускорителях принципиально понятна: разгоняют подходящие положительно заряженные остовы ядрер элементов электрическим полем до нужных скоростей и сталкивают их с мишенью, содержащей другие более тяжёлые элементы - происходят процессы слияния и распада атомных ядер различных элементов. Продукты этих процессов анализируют и делают выводы об образовании новых элементов.
Немецкие ученые из Центра по изучению тяжелых ионов Гельмгольца в серии экспериментов 2013-2014 годов планировали получить следующий, 119 элемент таблицы Менделеева, но потерпели неудачу. Они обстреливали ядра берклия (N=97) ядрами титана (N=22), однако анализ данных эксперимента не подтвердил наличия нового элемента.
В настоящее время можно считать идентифицированным существование ста восемнадцати химических элементов. Сообщения об обнаружении 119-го - первого элемента 8 периода - можно пока считать гипотетическим. Были заявления о синтезе элемента унбиквадий (124) и косвенные свидетельства об элементах унбинилий (120) и унбигексий (126), - но эти результаты ещё находятся в стадии подтверждения.
Сейчас, наконец, все, из официально известных и доказанных на сегодня 118 элементов, имеют утвержденные ИЮПАК общепризнанные названия. Не так давно самым тяжёлым из элементов, имеющих официально признанное название, был 116-й элемент, получивший его в мае 2012 года - ливерморий. Тогда же было официально утверждено название 114-го элемента - флеровий.
Сколько химических элементов вообще можно получить? Теоретически предсказывается возможность синтеза элементов с номерами 121-126. Это числа протонов в ядрах элементов. Проблема нижней границы таблицы Менделеева остаётся одной из важнейших в современной теоретической химии.
У каждого химического элемента имеется несколько изотопов. Изотопы - это атомы в ядрах которых имеется одинаковое число протонов, но разное количество нейтронов. Мир атомных ядер химических элементов очень разнообразен. Сейчас известно около 3500 ядер, отличающихся друг от друга либо числом протонов, либо числом нейтронов, либо тем и другим. Большинство из них получено искусственным путём. Вопрос очень интересный - сколько у данного элемента может быть изотопов?
Известно 264 ядра атомов, которые стабильны, то есть не испытывают со временем никаких быстрых самопроизвольных превращений. Распадов.
Остальные ядра в количестве 3236 подвержены различным видам радиоактивного распада: альфа-распаду (испускание альфа-частиц - ядер атома гелия); бета-распаду (одновременное испускание электрона и антинейтрино или позитрона и нейтрино, а также поглощение электрона с испусканием нейтрино); гамма-распаду (испускание фотонов - электромагнитных волн высокой энергии).
Из известных химических элементов периодической системы Менделеева, которые встречаются на Земле, только для 75 имеются точно и общепризнанно установленные авторы их открытия - обнаружение и идентификация. только при этих условиях - обнаружение и идентификация - признаётся факт открытия химического элемента.
В действительном открытии - выделение в чистом виде и изучении свойств - химических элементов, встречающихся в природе, участвовали учёные всего лишь девяти стран: Швеция (22 элемента), Англия (19 элементов), Франция (15 элементов), Германия (12 элементов). На Австрию, Данию, Россию, Швейцарию и Венгрию приходится открытие остальных 7 элементов.
Иногда указывают Испанию (платина) и Финляндию (иттрий - в 1794 году в шведском минерале из Иттербю финский химик Юхан Гадолин обнаружил оксид неизвестного элемента). Но платина, как благородный металл, была известна в самородном виде с древних времён - в чистом виде из руд платина была получена английским химиком У.Волластоном в 1803 году. Этот учёный более известен как открыватель минерала волластонита.
Металлический иттрий впервые получил в 1828 г. немецкий ученый Фридрих Велер.
Рекордсменом среди "охотников" за химическими элементами можно считать шведского химика К. Шееле - он обнаружил и доказал существование 6-ти химических элементов: фтора, хлора, марганца, молибдена, бария, вольфрама.
К достижениям в находках химических элементов этого учёного можно добавить ещё и седьмой элемент - кислород, но честь открытия которого он официально делит с английским учёным Дж. Пристли.
Второе место в открытии новых элементов принадлежит В.Рамзаю -
английскому или, точнее, шотландскому учёному: им открыты аргон, гелий, криптон, неон, ксенон. Кстати, открытие "гелия" очень любопытно. Это первое не "химическое" открытие химического элемента. Оно приписывается сейчас У.Рамзаю, но было сделано другими учёными. Так часто бывает.
18 августа 1868 года французский учёный Пьер Жансен, при полном солнечном затмении в индийском городе Гунтур, впервые исследовал хромосферу Солнца. Он настроил спектроскоп таким образом, что спектр короны Солнца удалось наблюдать не только при затмении, но и в обычные дни. Он выявил наряду с линиями водорода - синей, зелено-голубой и красной - яркую жёлтую линию, первоначально принятую им за линию натрия. Жансен написал об этом во Французскую академию наук.
Впоследствии было установлено, что эта ярко-жёлтая линия в солнечном спектре не совпадает с линией натрия и не принадлежит ни одному из ранее известных химических элементов.
Через 27 лет после этого первоначального открытия гелий был обнаружен на Земле - в 1895 году шотландский химик Уильям Рамзай, исследуя образец газа, полученного при разложении минерала клевеита, обнаружил в его спектре ту же ярко-жёлтую линию, найденную ранее в солнечном спектре. Образец был направлен для дополнительного исследования известному английскому учёному-спектроскописту Уильяму Круксу, который подтвердил, что наблюдаемая в спектре образца жёлтая линия совпадает с линией D3 гелия.
23 марта 1895 года Рамзай отправил сообщение о своём открытии гелия на Земле в Лондонское королевское общество, а также во Французскую академию через известного химика Марселена Бертло. так и получилось название этого химического элемента. От греческого наименования Солнца - гелиос. Первое открытие сделанное спектральным методом. Абсорбционная спектроскопия.
Во всех случаях у Рамзая были соавторы: В.Крукс (Англия) - гелий; В. Рэлей (Англия) - аргон; М. Траверс (Англия) - криптон, неон, ксенон.
По 4 элемента обнаружили:
И. Берцелиус (Швеция) - церий, селен, кремний, торий;
Г. Деви (Англия) - калий, кальций, натрий, магний;
П. Лекок де Буабодран (Франция) - галлий, самарий, гадолиний, диспрозий.
На долю России приходится открытие только одного из природных элементов: рутения (44). Название этого элемента происходит от позднелатинского названия России - Ruthenia. Этот элемент открыл профессор Казанского университета Карл Клаус в 1844 году.
Карл-Эрнст Карлович Клаус был русским химиком, автором ряда трудов по химии металлов платиновой группы, первооткрывателем химического элемента рутения. Он родился в 11 (22) января 1796 - 12 (24) марта 1864) в Дерпте, старинном русском городе Юрьеве (ныне Тарту), в семье художника. В 1837 году защитил диссертацию на степень магистра и был назначен адъюнктом по кафедре химии в Казанском университете. С 1839 года стал профессором химии Казанского университета, а с 1852 года – профессором фармации Дерптского университета. В 1861 году стал Членом-корреспондентом Петербургской Академии наук.
То, что большинство известных в природе химических элементов, было открыто учёными Швеции, Англии, Франции и Германии, вполне понятно - в 18-19 веках, когда и были открыты эти элементы, именно в данных странах был наиболее высокий уровень развития химии и химической технологии.
Ещё любопытен вопрос: а женщины-учёные открывали химические элементы?
Да. Но немного. Это Мария Складовская-Кюри, открывшая в 1898 году вместе с мужем П.Кюри полоний (название дано в честь её родины Польши) и радий, Лиза Мейтнер, принимавшая участие в открытии протактиния (1917 год), Ида Ноддак (Такке), обнаружившая в 1925 году совместно с будущим мужем В.Ноддаком рений, и Маргарита Перей, которая в 1939 году открыла франций и стала первой женщиной, избранной во Французскую академию наук.
В современной таблице Менделеева имеется несколько элементов, помимо рутения, названия которых связанны с Россией: самарий (63) - от названия минерала самарскита, открытого русским горным инженером В.М.Самарским в Ильменских горах, менделеевий (101); дубний (105). История названия этого элемента любопытна. Впервые этот элемент был получен на ускорителе в Дубне в 1970 году группой Г.Н.Флёрова путём бомбардировки ядер 243Am ионами 22Ne и независимо в Беркли (США) в ядерной реакции 249Cf + 15N = 260Db + 4n.
Советские исследователи предложили назвать новый элемент нильсборием (Ns), в честь великого датского учёного Нильса Бора, американцы - ганием (Ha), в честь Отто Гана, одного из авторов открытия спонтанного деления урана.
Рабочая группа ИЮПАК в 1993 году сделала вывод, что честь открытия элемента 105 должна быть разделена между группами из Дубны и Беркли. Комиссия ИЮПАК в 1994 году предложила название жолиотий (Jl), в честь Жолио-Кюри. До этого элемент официально назывался латинским числительным - уннилпентиумом (Unp), то есть просто 105-м элементом. Символы Ns, На, Jl можно и сейчас видеть в таблицах элементов, изданных в прежние годы. Например, на ЕГЭ по химии 2013 года. Согласно окончательному решению ИЮПАК в 1997 году этот элемент получил название "дубний" - в честь российского центра по исследованиям в области ядерной физики, наукограда Дубны.
В Объединенном институте ядерных исследований Дубны в разное время были впервые синтезированы сверхтяжелые химические элементы с порядковыми номерами 113–118. Элемент под номером 114 был назван "флеровий" - в честь Лаборатории ядерных реакций им. Г.Н.Флёрова Объединённого института ядерных исследований, где и был синтезирован этот элемент.
За последние 50 лет Периодическая система Д.И. Менделеева пополнилась 17 новыми элементами (102–118), из которых в ОИЯИ синтезировано 9. В том числе в последние 10 лет – 5 наиболее тяжелых (сверхтяжелых) элементов, замыкающих периодическую таблицу…
Впервые 114-й элемент - с "магическим" числом протонов (магические числа - ряд натуральных чётных чисел, соответствующих количеству нуклонов в атомном ядре, при котором становится полностью заполненной какая-либо его оболочка: 2, 8, 20, 28, 50, 82, 126 (последнее число - только для нейтронов) - был получен группой физиков под руководством Ю.Ц.Оганесяна в Объединённом институте ядерных исследований (Дубна, Россия) с участием учёных из Ливерморской национальной лаборатории (Ливермор, США; коллаборацией Дубна-Ливермор) в декабре 1998 года путём синтеза изотопов этого элемента посредством реакции слияния ядер кальция с ядрами плутония. Название 114-го элемента было утверждено 30 мая 2012 года: "флеровий" (Flerovium) и символическое обозначение Fl. Тогда же был назван 116 элемент – "ливерморий" (Livermorium) – Lv (кстати, время жизни этого элемента – 50 миллисекунд).
В настоящее время синтез трансурановых элементов в основном проводится в четырех странах: США, России, Германии и Японии. В России новые элементы получают в Объединенном институте ядерных исследований (ОИЯИ) в Дубне, в США - в Национальной лаборатории Оук-Ридж в Теннеси и Национальной лаборатории Лоуренса в Ливерморе, в Германии - в Центре по изучению тяжелых ионов Гельмгольца (он же - Институт тяжелых ионов) в Дармштадте, в Японии - в Институте физико-химических исследований (RIKEN).
За авторство создания 113-го элемента давно шла борьба между Японией и российско-американской группой ученых. Японские ученые во главе с Косукэ Моритой синтезировали 113-й элемент в сентябре 2004 года, разогнав на ускорителе и столкнув цинк-30 и висмут-83. Им удалось зафиксировать три цепочки распада, соответствующие цепочкам рождения 113-го элемента в 2004, 2005 и 2012 годах.
Российские и американские ученые объявили о создании 113-го элемента в процессе синтеза 115-го элемента в Дубне в феврале 2004 года и предложили назвать его беккерелием. По имени выдающегося физика Антуана Анри Беккереляя (фр. Antoine Henri Becquerel; 15 декабря 1852 - 25 августа 1908) - французский физик, лауреат Нобелевской премии по физике и один из первооткрывателей радиоактивности.
Наконец, в начале 2016 года в периодическую таблицу Менделеева официально добавлены названия четырёх новых химических элементов. Элементы с атомными номерами 113, 115, 117 и 118 верифицированы Международным союзом теоретической и прикладной химии (IUPAC).
Честь открытия 115-го, 117-го и 118-го элементов присуждена команде российских и американских ученых из Объединенного института ядерных исследований в Дубне, Ливерморской национальной лаборатории в Калифорнии и Окриджской национальной лаборатории в Теннесси.
До последнего времени эти элементы (113, 115, 117 и 118) носили не самые звучные названия унунтрий (Uut), унунпентий (Uup), унунсептий (Uus) и унуноктий (Uuo), однако в течение ближайших пяти месяцев первооткрыватели элементов смогут дать им новые, окончательные имена.
Открывателями 113-го элемента официально признаны ученые из японского Института естественных наук (RIKEN). В честь этого элемент рекомендовали назвать "японием". Право придумать названия остальным новым элементам предоставлено первооткрывателям, на что им отводилось пять месяцев, после чего их официально утвердит совет IUPAC.
115-й элемент предложено назвать "московием" в честь Подмосковья!
Свершилось! 8 июня 2016 года Международный союз теоретической и прикладной химии озвучил рекомендованные названия для 113-го, 115-го, 117-го и 118-го элементов таблицы Менделеева. Об этом сообщается на сайте союза.
Один из новых сверхтяжелых элементов таблицы Менделеева за номером 113 официально получил название "нихоний" и символ Nh. Соответствующее объявление сделал японский институт естественных наук "Рикэн", специалисты которого ранее открыли этот элемент.
Слово "нихоний" является производным от местного названия страны - "Нихон".
Международный союз теоретической и прикладной химии утвердил названия новым элементом за номерами 113, 115, 117 и 118 - нихоний(Nh), московий (Mc), тенессин (Ts) и оганессон (Og).
113-й элемент назван в честь Японии, 115-й - в честь Московской области, 117-й - по названию американского штата Теннеси, 118-й - в честь российского ученого академика РАН Юрия Оганесяна.
