Періодична система Менделєєва нова. Періодична система Менделєєва та періодичний закон.
У період ХІХ століття сильну реформацію зазнали багато напрямів, зокрема і хімія. Періодична системаМенделєєва, сформульована в 1869 році, призвела до єдиного розуміння залежності положення простих речовин у таблиці Менделєєва, яка встановила взаємозв'язок між відносною атомною масою, валентністю та властивістю елемента.
Доменделіївський період хімії
Дещо раніше, на початку дев'ятнадцятого століття, робилися неодноразові спроби систематизації Німецький хімік Деберейнер провів першу серйозну роботу з систематизації в галузі хімії. Він визначив, що ряд подібних речовин за властивостями можна поєднати в групи - тріади.
Помилковість уявлень німецького вченого
Суть представленого закону тріад Деберейнера визначалася тим, що атомна маса речовини, що шукається, близька до напівсуми (середнього значення) атомних мас двох останніх елементів таблиці тріади. Однак відсутність магнію в єдиній підгрупі кальцію, стронцію та барію було помилковим.
Цей підхід був наслідком штучного обмеження аналогічних речовин лише потрійними спілками. Деберейнер добре бачив схожість у хімічних параметрах фосфору та миш'яку, вісмуту та сурми. Однак він обмежив себе пошуком тріад. У результаті не зміг дійти правильної класифікації хімічних елементів.
Розділити існуючі елементи на тріади Деберейнеру, безумовно, не вдалося, закон явно вказував на присутність взаємозв'язку між властивостями і властивостями хімічних простих речовин.
Процес систематизації хімічних елементів
Усі подальші спроби систематизації спиралися на розподіл елементів залежно від своїх атомної маси. Надалі гіпотеза Деберейнера була використана іншими хіміками. З'явилося формування тріад, зошит та пентад (об'єднання у групи по три, чотири та п'ять елементів).
У другій половині ХІХ століття з'явилося одночасно кілька робіт, ґрунтуючись на яких Дмитро Іванович Менделєєв привів хімію до повноцінної систематизації хімічних елементів. Інша будова періодичної системи Менделєєва призвела до революційного розуміння та очевидності механізму розподілу простих речовин.
Періодична система елементів Менделєєва
На засіданні російської хімічної спільноти навесні 1869 було зачитано повідомлення російського вченого Д. І. Менделєєва про відкриття ним періодичного закону хімічних елементів.  Наприкінці цього ж року було опубліковано першу роботу «Основи хімії», до неї було включено першу періодичну систему елементів.
Наприкінці цього ж року було опубліковано першу роботу «Основи хімії», до неї було включено першу періодичну систему елементів.
У листопаді 1870 року він показав колегам доповнення «Природна система елементів та використання її для вказівки якостей невідкритих елементів». У цій праці Д. І. Менделєєв вперше використав термін « періодичний закон». Система елементів Менделєєва виходячи з періодичного закону визначала можливість існування не відкритих простих речовин, і чітко вказувала з їхньої властивості.
Виправлення та уточнення
У результаті 1971 року періодичний закон та елементів Менделєєва були доопрацьовані і доповнені російським хіміком.
В остаточній статті «Періодична законність хімічних елементів» вчений встановив визначення періодичного закону, де вказується, що характеристики простих тіл, властивості сполук, а також складних тіл, що ними утворюються, визначаються прямою залежністю згідно з їхньою атомною вагою.
Дещо пізніше, в 1872 році, будова періодичної системи Менделєєва було реорганізовано в класичний вид (короткоперіодний спосіб розподілу). 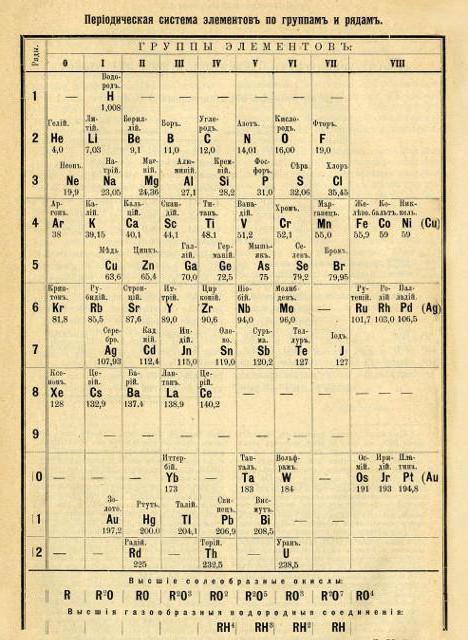
На відміну попередників, російський хімік повноцінно склав таблицю, ввів поняття закономірності атомної ваги хімічних елементів.
Характеристика елементів періодичної системи Менделєєва і виведені закономірності дозволили вченому описати властивості елементів, які ще відкриті. Менделєєв спирався на те, що властивості кожної речовини можна визначити згідно з характеристиками двох сусідніх елементів. Він назвав це правилом "зірки". Його суть у тому, що у таблиці хімічних елементів для визначення якості обраного елемента необхідно орієнтуватися по горизонталі та вертикалі у таблиці хімічних елементів.
здатна передбачити...
Таблиця елементів Менделєєва, попри свою точність і вірність, була визнана науковим товариством повноцінно. Деякі великі вчені зі світовим ім'ям відкрито висміювали можливість передбачити властивості відкритого елемента. І лише в 1885 році, після відкриття передбачуваних елементів - екаалюмінію, екабору та екасиліцію (галій, скандій та германій), нова класифікаційна система Менделєєва і періодичний закон були визнані як теоретичної основихімії.
На початку ХХ століття будова періодичної системи Менделєєва неодноразово коригувалося. У процесі отримання нових наукових даних Д. І. Менделєєв та його колега У. Рамзай дійшли висновку необхідність введення нульової групи. До її складу увійшли інертні гази (гелій, неон, аргон, криптон, ксенон та радон).
У 1911 році Ф. Содді вніс пропозицію розміщувати невиразні хімічні елементи - ізотопи - в одному осередку таблиці.
У процесі тривалої та копіткої роботи таблиця періодичної системи хімічних елементів Менделєєва була остаточно доопрацьована та набула сучасного вигляду. До її складу увійшло вісім груп та сім періодів. Групи – це вертикальні стовпці, періоди – горизонтальні. У групах визначено поділ на підгрупи. ![]()
Положення елемента в таблиці вказує на його валентність, чисто електрони та хімічні особливості. Як з'ясувалося пізніше, під час розробки таблиці Д. І. Менделєєвим було виявлено випадкове збіг кількості електронів елемента з його порядковим номером. ![]() Цей факт надалі спростив розуміння принципу взаємодії простих речовин та утворення складних. А також процес у зворотному напрямку. Розрахунок кількості отриманої речовини, а також необхідної для протікання хімічної реакції став теоретично доступним.
Цей факт надалі спростив розуміння принципу взаємодії простих речовин та утворення складних. А також процес у зворотному напрямку. Розрахунок кількості отриманої речовини, а також необхідної для протікання хімічної реакції став теоретично доступним.
Роль відкриття Менделєєва у сучасній науці
Система Менделєєва та її підхід до упорядкування хімічних елементів визначили подальший розвиток хімії. Завдяки правильному розумінню взаємозв'язку хімічних констант та аналізу Менделєєв зміг правильно скомпонувати та згрупувати елементи відповідно до їх властивостей.  Нова таблиця елементів дає можливість ясно і чітко розраховувати дані на початок проведення хімічної реакції, передбачати нові елементи та його властивості.
Нова таблиця елементів дає можливість ясно і чітко розраховувати дані на початок проведення хімічної реакції, передбачати нові елементи та його властивості.
Відкриття російського вченого вплинуло на подальший хід розвитку науки і технологій. Не існує технологічної галузі, яка б не задіяла знання хімії. Можливо, якби подібне відкриття не відбулося, то наша цивілізація пішла б іншим шляхом розвитку.
На даний час, офіційно міститься 118 хімічних речовин. З них 94 виявлені в природі, решта 24 отримана штучно в результаті ядерних реакцій. З усіх хімічних у природі знайдено 88; такі елементи, як технічний Tc, прометій Pm, астат Atта францій Fr, а також всі елементи, що йдуть за ураном U, вперше отримані штучно. У звичайних умовах відповідні прості речовини для 11 елементів є газами, для 2 – рідинами, інших елементів – твердими тілами.
Варто прочитати
 Дмитро Іванович Менделєєв- Російський учений-енциклопедист, громадський діяч. Хімік, фізикохімік, фізик, метролог, економіст, технолог, геолог, метеоролог, педагог, повітроплавець, приладобудівник. Професор Санкт-Петербурзького університету; член-кореспондент із розряду «фізичний» Імператорської Санкт-Петербурзької Академії наук. Серед найбільш відомих відкриттів- Періодичний закон хімічних елементів, один з фундаментальних законів світобудови, невід'ємний для всього природознавства.
Дмитро Іванович Менделєєв- Російський учений-енциклопедист, громадський діяч. Хімік, фізикохімік, фізик, метролог, економіст, технолог, геолог, метеоролог, педагог, повітроплавець, приладобудівник. Професор Санкт-Петербурзького університету; член-кореспондент із розряду «фізичний» Імператорської Санкт-Петербурзької Академії наук. Серед найбільш відомих відкриттів- Періодичний закон хімічних елементів, один з фундаментальних законів світобудови, невід'ємний для всього природознавства.
Періодична система хімічних елементів- Класифікація хімічних елементів, що встановлює залежність різних властивостей елементів від заряду атомного ядра. Система є графічним виразом періодичного закону, встановленого російським хіміком Д.І. Менделєєвим у 1869 році. Її первісний варіант розробили Д.І. Менделєєвим у 1869-1871 роках і встановлював залежність властивостей елементів від їхньої атомної ваги. Усього запропоновано кілька сотень варіантів зображення періодичної системи. У сучасному варіанті системи передбачається зведення елементів у двовимірну таблицю, в якій кожен стовпець визначає основні фізико-хімічні властивості, а рядки є періодами, певною мірою подібними один одному. До середини XIX століття було відкрито 63 хімічні елементи, і спроби знайти закономірності в цьому наборі робилися неодноразово. Найпоширенішими є 3 форми таблиці Менделєєва: «коротка», «довга» і «наддовга». У «наддовгому» варіанті кожен період займає рівно один рядок. Періодична система Д.І. Менделєєва стала найважливішою віхою у розвитку атомно-молекулярного вчення.
У таблицю Менделєєва вписано новий елемент
Одні з найпопулярніших хімічних питань: "Скільки зараз відомо хімічних елементів?", "Скільки існує хімічних елементів?", "Хто їх відкрив?"
Ці питання не мають простої та однозначної відповіді.
Що означає "відомо"? Зустрічаються у природі? На землі, у воді, у космосі? Отримано та вивчено їх властивості? Властивості чого? Речовини у вигляді фаз або лише на атомно-молекулярному рівні? Наявні сучасні технологіїдозволяють виявляти і кілька атомів... Але, за окремим атомом властивості речовини не визначити.
А що означає "існують"? У практичному плані це зрозуміло: є в природі в такій кількості і стільки часу, щоб вони та їх сполуки могли реально впливати на природні явища. Або хоча б можна було вивчити їхні властивості у лабораторії.
Таких хімічних елементів у природі виявлено близько 90. Чому близько? Тому що серед елементів із порядковим номером менше 92 (до урану) у природі відсутні технецій (43) та францій (87). Практично немає астату (85). З іншого боку, і нептуній (93) і плутоній (94) (нестабільні трансуранові елементи) виявляються у природі там, де трапляються уранові руди. Всі елементи наступні після плутонію Pu в періодичній системі Д. І. Менделєєва в земній корі повністю відсутні, хоча деякі з них, безсумнівно, утворюються в космосі під час вибухів наднових зірок. Але довго вони не живуть.
До цього часу вчені синтезували 26 трансуранових елементів, починаючи з нептунія (N=93) і закінчуючи елементом з номером N=118 (номер елемента відповідає числу протонів в ядрі атома та електронів навколо ядра атома).
Трансуранові хімічні елементи від 93 до 100 одержують у ядерних реакторах, інші - в результаті ядерних реакцій на прискорювачах частинок. Технологія отримання трансуранових елементів на прискорювачах важливо зрозуміла: розганяють відповідні позитивно заряджені кістяки ядрер елементів електричним полем до необхідних швидкостей і зіштовхують їх із мішенню, що містить інші важчі елементи - відбуваються процеси злиття і розпаду атомних ядер різних елементів. Продукти цих процесів аналізують та роблять висновки про утворення нових елементів.
Німецькі вчені з Центру з вивчення важких іонів Гельмгольця у серії експериментів 2013-2014 років планували отримати наступний, 119 елемент таблиці Менделєєва, але зазнали невдачі. Вони обстрілювали ядра берклію (N=97) ядрами титану (N=22), проте аналіз даних експерименту не підтвердив наявності нового елемента.
Нині вважатимуться ідентифікованим існування ста вісімнадцяти хімічних елементів. Повідомлення про виявлення 119-го - першого елемента 8 періоду - можна вважати гіпотетичним. Були заяви про синтез елемента унбіквадій (124) та непрямі свідоцтва про елементи унбінілій (120) та унбігексій (126), але ці результати ще перебувають у стадії підтвердження.
Зараз, нарешті, усі, з офіційно відомих та доведених на сьогодні 118 елементів, мають затверджені ІЮПАК загальновизнані назви. Нещодавно найважчим із елементів, що мають офіційно визнану назву, був 116-й елемент, який отримав його в травні 2012 року - ліверморій. Тоді ж було офіційно затверджено назву 114-го елемента – флеровий.
Скільки хімічних елементів можна отримати? Теоретично передбачається можливість синтезу елементів із номерами 121-126. Це числа протонів у ядрах елементів. Проблема нижньої межі таблиці Менделєєва залишається однією з найважливіших у сучасній теоретичній хімії.
Кожен хімічний елемент має кілька ізотопів. Ізотопи - це атоми в ядрах яких є однакова кількість протонів, але різна кількість нейтронів. Світ атомних ядер хімічних елементів дуже різноманітний. Зараз відомо близько 3500 ядер, що відрізняються один від одного або числом протонів, або нейтронів, або тим і іншим. Більшість їх отримано штучним шляхом. Питання дуже цікаве - скільки у даного елемента може бути ізотопів?
Відомо 264 ядра атомів, які стабільні, тобто не зазнають згодом жодних швидких мимовільних перетворень. Розпадів.
Інші ядра в кількості 3236 схильні різним видамрадіоактивного розпаду: альфа-розпаду (випускання альфа-часток - ядер атома гелію); бета-розпаду (одночасне випромінювання електрона та антинейтрино або позитрону та нейтрино, а також поглинання електрона з випромінюванням нейтрино); гамма-розпаду (випускання фотонів – електромагнітних хвиль високої енергії).
З відомих хімічних елементів періодичної системи Менделєєва, що зустрічаються Землі, лише 75 є точно і загальновизнано встановлені автори їх відкриття - виявлення та ідентифікація. лише за цих умов - виявлення та ідентифікація - визнається факт відкриття хімічного елемента.
У дійсному відкритті - виділення в чистому вигляді та вивченні властивостей - хімічних елементів, що зустрічаються в природі, брали участь вчені лише дев'яти країн: Швеція (22 елементи), Англія (19 елементів), Франція (15 елементів), Німеччина (12 елементів). На Австрію, Данію, Росію, Швейцарію та Угорщину доводиться відкриття решти 7 елементів.
Іноді вказують Іспанію (платина) та Фінляндію (іттрій – у 1794 році у шведському мінералі з Ітербю фінський хімік Юхан Гадолін виявив оксид невідомого елементу). Але платина, як шляхетний метал, була відома у самородному вигляді з давніх часів - у чистому вигляді з руд платина була отримана англійським хіміком У. Волластоном у 1803 році. Цей учений найбільш відомий як відкривач мінералу волластоніту.
Металевий ітрій вперше отримав у 1828 р. німецький вчений Фрідріх Велер.
Рекордсменом серед "мисливців" за хімічними елементами можна вважати шведського хіміка К. Шееле - він виявив та довів існування 6-ти хімічних елементів: фтору, хлору, марганцю, молібдену, барію, вольфраму.
До досягнень у знахідках хімічних елементів цього вченого можна додати ще й сьомий елемент – кисень, але честь відкриття якого він офіційно ділить з англійським вченим Дж. Прістлі.
Друге місце у відкритті нових елементів належить В.Рамзаю -
англійській чи, точніше, шотландському вченому: їм відкриті аргон, гелій, криптон, неон, ксенон. До речі, відкриття "гелію" дуже цікаве. Це перше не "хімічне" відкриття хімічного елемента. Воно приписується зараз У.Рамзаю, але зроблено іншими вченими. Так часто буває.
18 серпня 1868 року французький вчений П'єр Жансен, при повному сонячному затемненнів індійському місті Гунтур вперше досліджував хромосферу Сонця. Він налаштував спектроскоп таким чином, що спектр корони Сонця вдалося спостерігати не лише за затемнення, а й у звичайні дні. Він виявив поряд з лініями водню – синьою, зелено-блакитною та червоною – яскраву жовту лінію, спочатку прийняту ним за лінію натрію. Жансен написав про це у Французьку академію наук.
Згодом було встановлено, що ця яскраво-жовта лінія в сонячному спектрі не збігається з лінією натрію і не належить до жодного з раніше відомих хімічних елементів.
Через 27 років після цього початкового відкриття гелій було виявлено на Землі - в 1895 році шотландський хімік Вільям Рамзай, досліджуючи зразок газу, отриманого при розкладанні мінералу клевеїта, виявив у його спектрі ту ж яскраво-жовту лінію, знайдену раніше в сонячному. Зразок був направлений для додаткового дослідження відомому англійському вченому-спектроскопісту Вільяму Круксу, який підтвердив, що жовта лінія, що спостерігається в спектрі зразка, збігається з лінією D3 гелію.
23 березня 1895 року Рамзай відправив повідомлення про своє відкриття гелію на Землі до Лондонського королівського товариства, а також до Французької академії через відомого хіміка Марселена Бертло. так і вийшла назва цього хімічного елемента. Від грецької назви Сонця – геліос. Перше відкриття зроблене спектральним методом. Абсорбційна спектроскопія.
У всіх випадках у Рамзая були співавтори: В. Крукс (Англія) – гелій; В. Релей (Англія) – аргон; М. Траверс (Англія) – криптон, неон, ксенон.
По 4 елементи виявили:
І. Берцеліус (Швеція) – церій, селен, кремній, торій;
Г. Деві (Англія) – калій, кальцій, натрій, магній;
П. Лекок де Буабодран (Франція) – галій, самарій, гадоліній, диспрозій.
Перед Росії припадає відкриття лише з природних елементів: рутенія (44). Назва цього елемента походить від пізньолатини назви Росії - Ruthenia. Цей елемент відкрив професор Казанського університету Карл Клаус у 1844 році.
Карл-Ернст Карлович Клаус був російським хіміком, автором низки праць з хімії металів платинової групи, першовідкривачем хімічного елемента рутенію. Він народився в 11 (22) січня 1796 - 12 (24) березня 1864) у Дерпті, старовинному російському місті Юр'єві (нині Тарту), у родині художника. В 1837 захистив дисертацію на ступінь магістра і був призначений ад'юнктом на кафедрі хімії в Казанському університеті. З 1839 став професором хімії Казанського університету, а з 1852 - професором фармації Дерптського університету. У 1861 став Членом-кореспондентом Петербурзької Академії наук.
Те, що більшість відомих у природі хімічних елементів було відкрито вченими Швеції, Англії, Франції та Німеччини, цілком зрозуміло - у 18-19 століттях, коли і були відкриті ці елементи, саме в цих країнах був найвищий рівень розвитку хімії та хімічної технології .
Ще цікаве питання: а жінки-вчені відкривали хімічні елементи?
Так. Але небагато. Це Марія Складовська-Кюрі, яка відкрила в 1898 році разом із чоловіком П.Кюрі полоній (назва дано на честь її батьківщини Польщі) і радій, Ліза Мейтнер, яка брала участь у відкритті протактінія (1917 рік), Іда Ноддак (Такке), що виявила в 1925 спільно з майбутнім чоловіком В.Ноддаком реній, і Маргарита Перей, яка в 1939 відкрила Франції і стала першою жінкою, обраною до Французької академії наук.
У сучасній таблиці Менделєєва є кілька елементів, крім рутенію, назви яких пов'язані з Росією: самарій (63) - від назви мінералу самарскіту, відкритого російським гірським інженером В.М.Самарським в Ільменських горах, Менделєєвій (101); дубні (105). Історія назви цього елемента цікава. Вперше цей елемент був отриманий на прискорювачі в Дубні в 1970 році групою Г.Н.Флерова шляхом бомбардування ядер 243Am іонами 22Ne і незалежно в Берклі (США) в ядерній реакції 249Cf + 15N = 260Db + 4n.
Радянські дослідники запропонували назвати новий елемент нільсборієм (Ns), на честь великого датського вченого Нільса Бора, американці - ганієм (Ha), на честь Отто Гана, одного з авторів відкриття спонтанного поділу урану.
Робоча група ІЮПАК 1993 року зробила висновок, що честь відкриття елемента 105 має бути розділена між групами з Дубни та Берклі. Комісія ІЮПАК у 1994 році запропонувала назву жоліотій (Jl), на честь Жоліо-Кюрі. До цього елемент офіційно називався латинським чисельним - Унілпентіум (Unp), тобто просто 105-м елементом. Символи Ns, На, Jl можна й зараз бачити у таблицях елементів, виданих у роки. Наприклад, на ЄДІ з хімії 2013 року. Згідно з остаточним рішенням ІЮПАК у 1997 році цей елемент отримав назву "дубний" - на честь російського центру з досліджень у галузі ядерної фізики, наукограда Дубни.
В Об'єднаному інституті ядерних досліджень Дубни у різний час було вперше синтезовано надважкі хімічні елементи з порядковими номерами 113–118. Елемент під номером 114 було названо "флеровим" - на честь Лабораторії ядерних реакцій ім. Г.Н.Флёрова Об'єднаного інституту ядерних досліджень, де й синтезували цей елемент.
Останні 50 років Періодична система Д.І. Менделєєва поповнилася 17 новими елементами (102–118), з яких в ОІЯД синтезовано 9. У тому числі в останні 10 років – 5 найважчих (надважких) елементів, що замикають періодичну таблицю…
Вперше 114-й елемент - з "магічним" числом протонів (магічні числа - ряд натуральних парних чисел, що відповідають кількості нуклонів в атомному ядрі, при якому стає повністю заповненою будь-яка його оболонка: 2, 8, 20, 28, 50, 82 , 126 (останнє число - тільки для нейтронів) - було отримано групою фізиків під керівництвом Ю.Ц.Оганесяна в Об'єднаному інституті ядерних досліджень (Дубна, Росія) за участю вчених з Ліверморської національної лабораторії (Лівермор, США; колаборацією Дубна-Лівермор) У грудні 1998 року шляхом синтезу ізотопів цього елемента за допомогою реакції злиття ядер кальцію з ядрами плутонію Назва 114-го елемента була затверджена 30 травня 2012 року: "флеровий" (Flerovium) і символічне позначення Fl. (Livermorium) – Lv (до речі, час життя цього елемента – 50 мілісекунд).
В даний час синтез трансуранових елементів в основному проводиться в чотирьох країнах: США, Росії, Німеччині та Японії. У Росії нові елементи отримують в Об'єднаному інституті ядерних досліджень (ОІЯД) у Дубні, у США – у Національній лабораторії Оук-Рідж у Теннесі та Національній лабораторії Лоуренса у Ліверморі, у Німеччині – у Центрі з вивчення важких іонів Гельмгольця (він же – Інститут важких іонів) у Дармштадті, в Японії – в Інституті фізико-хімічних досліджень (RIKEN).
За авторство створення 113-го елемента давно точилася боротьба між Японією та російсько-американською групою вчених. Японські вчені на чолі з Косуке Морітою синтезували 113-й елемент у вересні 2004 року, розігнавши на прискорювачі і зіштовхнувши цинк-30 та вісмут-83. Їм вдалося зафіксувати три ланцюжки розпаду, що відповідають ланцюжкам народження 113-го елемента у 2004, 2005 та 2012 роках.
Російські та американські вчені оголосили про створення 113-го елемента в процесі синтезу 115-го елемента в Дубні у лютому 2004 року та запропонували назвати його беккерелієм. По імені видатного фізикаАнтуана Анрі Беккереляя (фр. Antoine Henri Becquerel; 15 грудня 1852 - 25 серпня 1908) - французький фізик, лауреат Нобелівської премії з фізики та один із першовідкривачів радіоактивності.
Нарешті, на початку 2016 року до періодичної таблиці Менделєєва офіційно додано назви чотирьох нових хімічних елементів. Елементи з атомними номерами 113, 115, 117 та 118 верифіковані Міжнародним союзом теоретичної та прикладної хімії (IUPAC).
Честь відкриття 115-го, 117-го та 118-го елементів присуджено команді російських та американських учених з Об'єднаного інституту ядерних досліджень у Дубні, Ліверморській національній лабораторії у Каліфорнії та Окріджській національній лабораторії у Теннессі.
До останнього часу ці елементи (113, 115, 117 і 118) носили не найзвучніші назви унунтрій (Uut), унунпентій (Uup), унунсептій (Uus) і унуноктій (Uuo), однак протягом найближчих п'яти місяців першовідкривачі елементів нові, остаточні імена.
Відкривачами 113-го елементу офіційно визнано вчених із японського Інституту природничих наук (RIKEN). На честь цього елемент рекомендували назвати "японією". Право придумати назви решти нових елементів надано першовідкривачам, на що їм відводилося п'ять місяців, після чого їх офіційно затвердить рада IUPAC.
115-й елемент запропоновано назвати "московієм" на честь Підмосков'я!
Здійснилося! 8 червня 2016 року Міжнародний союзтеоретичної та прикладної хімії озвучив рекомендовані назви для 113-го, 115-го, 117-го та 118-го елементів таблиці Менделєєва. Про це повідомляє сайт союзу.
Один із нових надважких елементів таблиці Менделєєва за номером 113 офіційно отримав назву "ніхоній" та символ Nh. Відповідне оголошення зробив японський інститут з природничих наук "Рікен", фахівці якого раніше відкрили цей елемент.
Слово "ніхоній" є похідним від місцевої назви країни - "Ніхон".
Міжнародний союз теоретичної та прикладної хімії затвердив назви новим елементом за номерами 113, 115, 117 та 118 - ніхоній(Nh), московський (Mc), тенессин (Ts) та оганессон (Og).
113-й елемент названий на честь Японії, 115-й – на честь Московської області, 117-й – за назвою американського штату Теннесі, 118-й – на честь російського вченого академіка РАН Юрія Оганесяна.
Сергію, мабуть Ви молоді і не відчуваєте себе частиною нашої країни. Зрозуміло, якщо молоді, але не викликає поваги, якщо Ви – "громадянин Москви".
1. "Як же мені набридли дивані політичні експерти, хвальки та невиховані вискочки, які поїхали жити в інші країни, а тепер за будь-якої нагоди намагаються відсипати "компліментів" своїм колишнім співвітчизникам."
Та хрін із ними, вони нас не цікавлять у нас свої шкурні інтереси – як НАМ жити. Хоч і шкода втратити таких. Це люди, які, як мінімум, не побоялися зірватися і почати життя з чистого аркуша і низу соціальних сходів.
2. “І агресії жителів України теж не розумію. І жителів інших країн. А вам би все про "москалів" зуби поскалити. Самовиражатися можна і в інших областях, а не тільки ображаючи інших людей в Інтернеті.
Гм... У вихованих у совку, нормально вихованих, у підкірці сидить: "Вставай країна величезна..." коли ворог входить на нашу землю. Слава аллаху і будде, що хохли – індивідуалісти та чхати переважно хотіли на свою країну. Ось і срут в інтернеті або обматерять клятого москаля замість повноцінної війни за свій шматок землі... А Ви б який варіант віддали перевагу?
3. "Те, що відбувається між нашими політиками - це одне." Не треба п....ть!! "Маленькі звитяжні війни" на те і розраховані, щоб викликати патріотичний чад у маленьких людей! Підтримка Путіна 87% цілком реальна, принаймні до падіння рубля! І саме ці 87% відповідальні за те, що відбувається з рештою 13% і з нашими сусідами: братами грузинами, братами українцями.
4. Найголовніше.
Навіть хохли можуть забити болт на втрату частини території, на утиск его та яєць. А нам тут жити. І Ви, Сергію, мабуть не знаєте історії своєї сім'ї, або вона стояла осторонь того, що у нас діялася.
А моя сім'я протягом багатьох поколінь кров'ю впаяна в цю землю. Лише за 20 століття: воювали 6 мужиків у 3 війнах, двоє не повернулися. 4 жінок та дітей від голоду померли. Розкучували. У таборах згинули 4 особи. Один атомну зброю випробовував, помер від раку. Його син у 24 роки помер через наслідки опромінення батька. Двоє вчених у роді, керівники хімічної та енергетичної промисловості, лікарі вищої категорії, вчитель, військовослужбовець, палац Аміна, що штурмував.
І заради чого все це? Люди творили майбутнє, без дурнів не шкодуючи себе і здоров'я, або ж виживали заради дітей. І що ми бачимо? Та хрін з нею, з бідністю. Але тотально губиться спадщина предків. Де і як наші діти житимуть? Нормою стало кидалове на державному рівні. За федеральними програмами фінансування "Чиста вода" треба готівкою повертати до 30%!! Молодь тупа і безграмотна. Найпростіший конкурс на рахувати-писати-фізика-математика проходять 0,3-0,7% випускників технічних ВНЗ! З кого готувати інженерів, вчених-прикладників?
Чи багато російських новинза 2015 рік, для нас радісні? Викинули із чергової міжнародної програми? Чергове фі від інших країн? Черговий обвал рубля? Чергове згортання виробництва та ринку загалом?
Мало хто з дорослих знає, скільки елементів у таблиці Менделєєва. Крім того, ваші знання можуть бути застарілими.
Справа в тому, що таблиця досі знаходиться в відкритої формітобто не закінчена, тому що не всі її складові відомі.
Якби хіміка запитали про кількість відомих елементівнаприкінці XVII століття, то він з упевненістю сказав би, що їх 21. І навіть коли Менделєєв розробив класифікацію хімічних елементів (1869-1871 рр.), що використовується до наших днів, їх було відкрито всього 63.
Спроби систематизації робилися неодноразово, але дуже важко будувати висновки про цілому з його частини і більше шукати у ньому закономірності.
Труднощі полягали саме в тому, що в той час вчені не уявляли, що їм відома лише половина ланок з існуючого ланцюга.
Щойно вчені та дослідники не намагалися побудувати відому їм половину таблиці. Цим займалися як хіміки, а й музиканти, які шукають систему за законом октав.
У Ньюлендса майже вийшло, але він сам себе скомпрометував містичним підґрунтям, майже знайденим ним у хімії музичної гармонії. Тільки через кілька років після цього було створено відому нам таблицю, кількість складових у якій поступово збільшувалася до теперішнього часу.
Можливо, система у властивостях цих 63 елементів і виявилася, згідно з легендою, Менделєєвим уві сні, але сам він казав, що це сталося не раптово, не по клацанню пальців. Щоб знайти закономірності, він думав майже 20 років. Причому їм залишили порожні місця для невідкритих ще ланок цього довгого ланцюжка.
Подальше розширення
До кінцю XIXстоліття таблицю заповнювали вже 84 елементи (розвивається спектроскопія надала відкриттям новий імпульс), а до середини XX століття додалися ще 13. Тому школярі в 1950 могли з упевненістю заявляти, що в періодичній таблиці 97 компонентів.
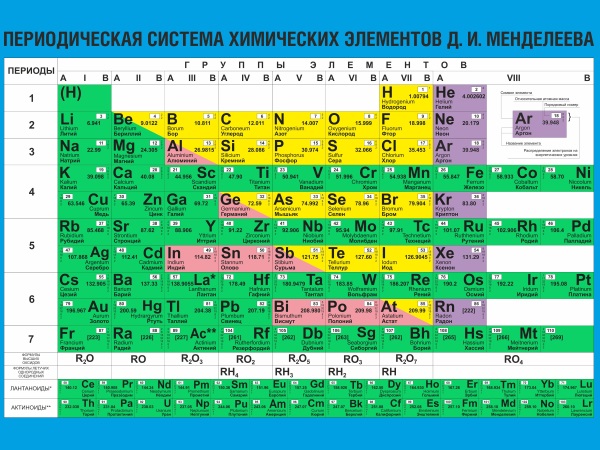
Таблиця Менделєєва.
З того часу елементи під номерами від 98-го поступово відкривалися та розширювали таблицю після початку використання атомної енергії. Так, у 2011 році були заповнені вже 114-й і 116-й осередок.
На початку 2016 року в таблиці знову відбулося поповнення — до неї додалися 4 нові елементи, хоча відкриті вони були значно раніше.
Їхні атомні номери 113, 115, 117 і 118, причому один з хімічних елементів японського походження (робоча назва ununtrium, або скорочено Uut). Це відкриття дозволило нарешті хімікам Японії поряд з іншими потрапити в періодичну таблицю, розташувавши своє відкриття в 113-му осередку.
Інші елементи відкриті російсько-американською групою:
- ununpentium, або Uup (115);
- ununseptium, або Uus (117);
- ununoctium, або Uuo (118).
Це тимчасові назви, і в другій половині 2016 року у таблиці з'являться їхні реальні імена та скорочені позначення із 2 літер. Право вибрати імена належить першовідкривачам. На чому вони зупиняться, поки що невідомо.
Назви можуть бути пов'язані з міфологією, астрономією, географією чи це можуть бути терміни з хімії, а може, імена вчених.
Скільки їх всього?
Навіть якщо точно знати, скільки елементів міститься в менделєєвській таблиці, можна відповісти двояко, причому обидві відповіді будуть правильні.
Справа в тому, що ця таблиця має дві версії. В одній міститься 118 компонентів, а в другій 126.
Різниця між ними в тому, що в першому варіанті вже відкриті та офіційно прийняті науковими колами компоненти, а в другому вписані також і гіпотетичні, тобто існуючі тільки на папері та в умах вчених. Вони можуть бути отримані завтра, а можуть і за 100 років.
А ось у 118-елементному варіанті всі компоненти реально існують. З них 94 виявлено в природі, решту отримано лабораторно. Проте другий варіант теж має право на існування, тому що природа любить порядок.
Якщо закономірність показує, що у наявних хімічних елементів має бути продовження, отже, рано чи пізно воно з'явиться завдяки новим, поки що не відомим технологіям.
